您搜索的關鍵詞為:
您搜索的關鍵詞為:
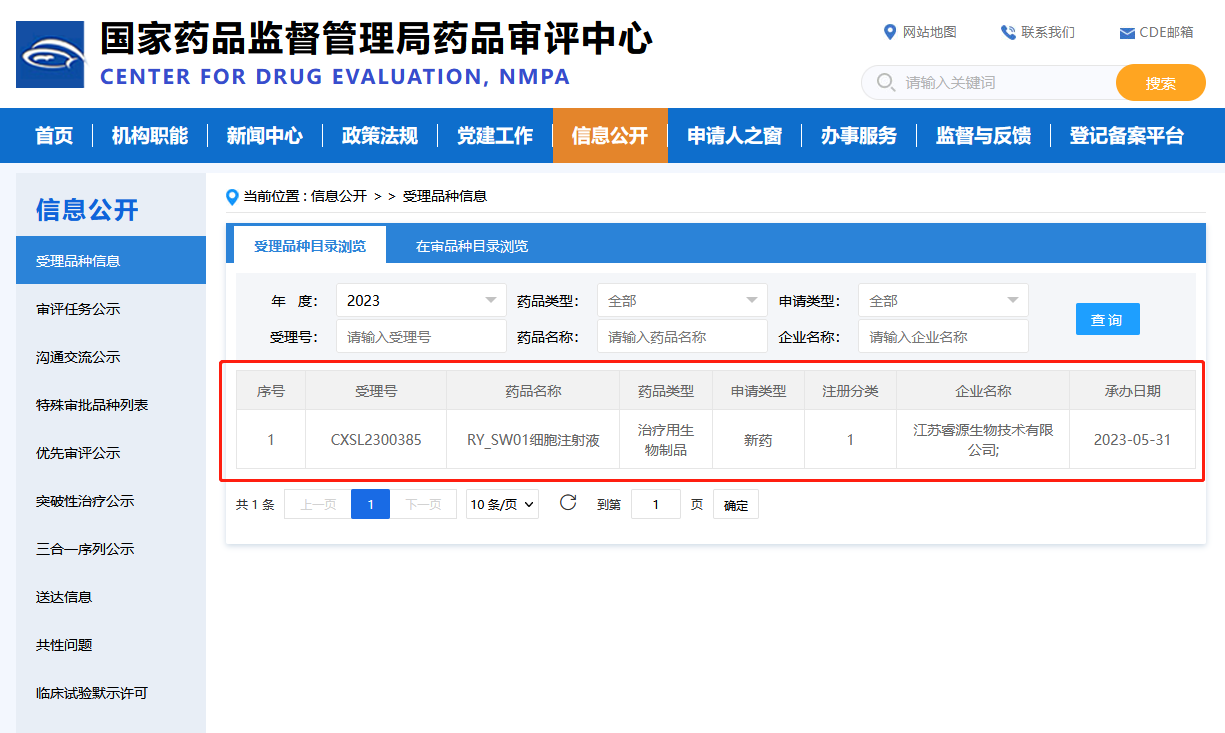
5月31日,江蘇睿源生物技術有限公司研發的生物制品1類新藥“RY_SW01細胞注射液”的第2項臨床試驗申請(IND),正式取得中國國家藥品監督管理局藥品審評中心(CDE)的受理(受理號為:CXSL2300385)。
干細胞是一種可以自我更新以及分化的細胞,具有獨特的自我復制能力和再生發育成各類組織器官的潛能,這一特性使其成為潛在用于醫學治療的重要工具。近年來,全球已獲批十余種間充質干細胞產品,但國內尚無干細胞新藥獲批上市。
公司自成立之日起,始終聚焦間充質干細胞的成藥性開發,開展了大量的臨床研究、基礎研究和新藥研發工作。目前,公司自主研發的1類新藥“RY_SW01細胞注射液”已于2022年9月獲得治療“活動性狼瘡腎炎”的Ⅰ/Ⅱ期臨床批件,正在開展多中心臨床試驗中。
此次關于第二項適應癥的臨床試驗申報,進一步彰顯了公司在干細胞藥物開發中的創新速度與實力。下一步,睿源生物將乘勢而上,加快新藥研發進度,持續完善多管線布局,規范開展臨床試驗,力爭早日實現干細胞從臨床治療技術到標準化藥物的轉化。
 蘇公網安備:32100302010738號
蘇公網安備:32100302010738號電話:0514-89993100 傳真:0514-89993100 郵件: